|
1.はじめに
薬事法の申請等に係る資料及び原資料を作成する際に,電磁的記録及び電子署名を利用する場合には,電磁的記録・電子署名の要件(以下,ER/ES
要件)を満足する必要がある。ER/ES 要件は,GxP の領域を問わず適用される要件であり,日米欧の各当局から規制やガイドラインが発行されている。本稿では各極のER/ES
要件を整理したうえで,主要なER/ES 要件についてeCTD でどのように対応すべきかを述べることとする。
2.各極のER/ES 要件
各極のER/ES 要件を示す主な規制・ガイドラインを表1
に示す。
表1 ER/ES 規制・ガイドライン発行状況

2.1 21 CFR Part 11
ER/ES要件は,米国Food and Drug
Administration(FDA)から 1997 年に発効された 21 CFR Part
11“ Electronic Records ; Electronic Signatures”(以下,Part
11) で, 初めて示された。その後,要件の解釈が拡大傾向にあることを踏まえ,FDA は2003
年に“Electronic Records; Electronic Signatures-Scope
and Application” を発行し,適用範囲を狭め,Part 11 発効以前のシステムを適用除外とするとともに,いくつかの要件(バリデーション,監査証跡,電子記録のコピー,電子記録の保管)の執行を査察官の裁量に任せ,規制の文言を杓子定規に適用しないという意図を明確にした。その後,改訂の噂は何度かあったものの,参照規制や事務的な内容の変更のみで,ER/ES
要件自体は変わっていない。最近では,GCP 領域向けに,最新の業界・技術動向を踏まえて2024
年に新たなガイダンス“Electronic Systems, Electronic Records,
and Electronic Signatures in Clinical Investigations
Questions and Answers”が発行されたところである。
2.2 ER/ES 指針
日本では,厚生労働省から2005 年に「医薬品等の承認又は許可等に係る申請等における電磁的記録及び電子署名の利用について」(以下,ER/ES
指針)が発行されており,その構成・内容はPart 11 に近いものとなっている。
ER/ES 指針に示されるER/ES 要件を表2 に示すが,電磁的記録の要件を真正性,見読性,保存性に分けて記載されている。また電子署名は,電子署名法(電子署名及び認証業務に関する法律(平成12
年5 月31 日法律第102 号))に基づくことが期待されている。
表2 ER/ES 指針のER/ES 要件

2.3 EMA のガイドライン
欧州European Medicines Agency(EMA)
からは領域別にER/ES 要件を盛り込んだガイダンスが発行されている。GMP 領域ではEU
のGMP ガイダンスの付属書Annex 11 Computerised System(以下,Annex
11)が2011 年に改訂されている。なおAnnex 11 を含むこのGMP ガイダンスはPharmaceutical
Inspection Scheme(PIC/S)でも採用されており,我が国を含むPIC/S
加盟国において遵守することが期待されている。GCP 領域では2022 年に発行された“Guideline
on computerised systems and electronic data in
clinical trials”(以下,EMA ガイド)がER/ES 要件を詳細に展開している。
2.4 三極ガイドラインのER/ES 要件比較
日米欧三極の規制・ガイドラインのER/ES
要件の比較を表3 に示す。
表3 日米欧三極の規制・ガイドラインのER/ES
要件比較
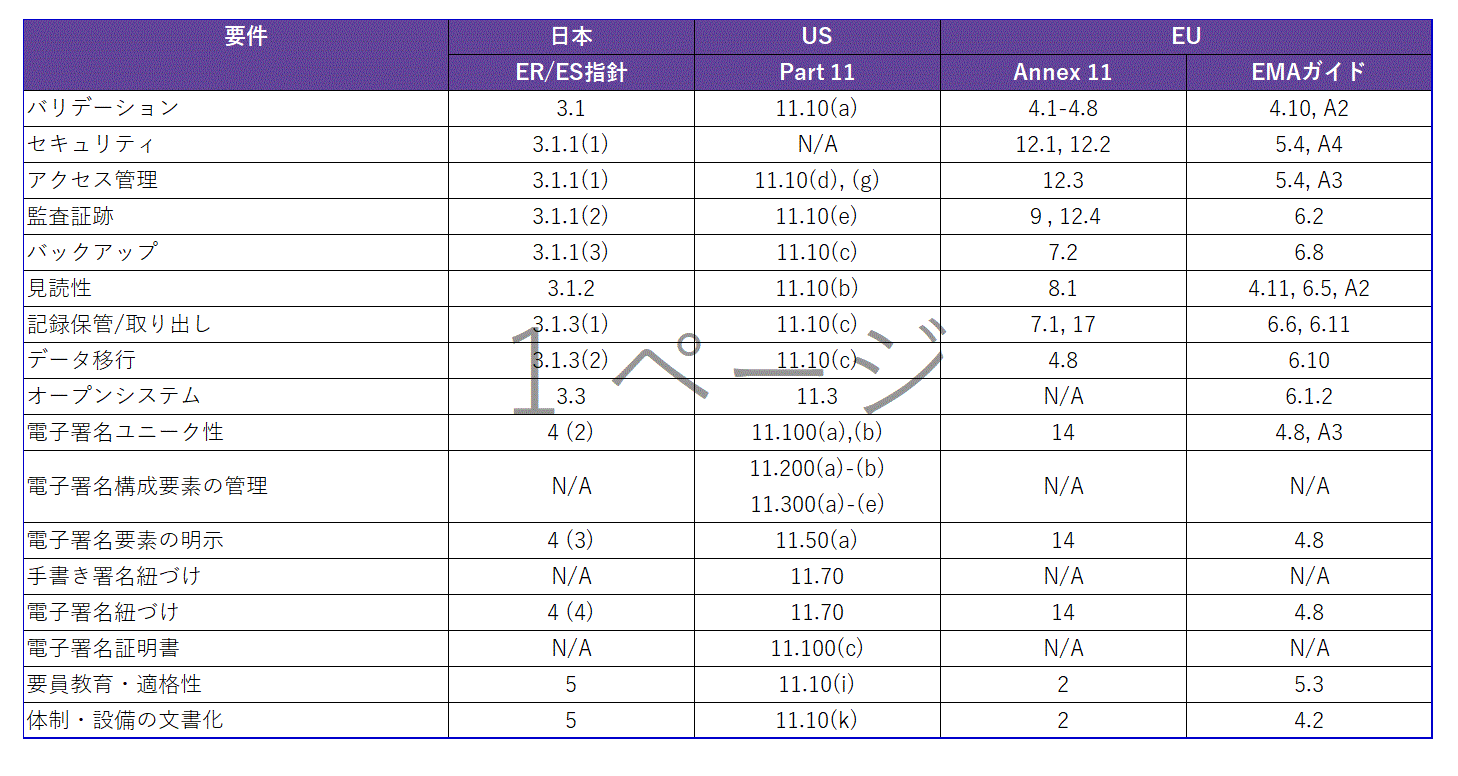
表に見るように,各ガイダンスにおいて重要なER/ES要件に大きな違いはないことから,本稿では日本のER/ES
指針の要件を中心に論を進める。
ちなみに各極当局からER/ES 要件を含む規制・ガイドラインが不定期に発行・更新されているが,そこには同じような要件であっても異なる粒度で,微妙に異なる表現で記述されていることが多い。これらのER/ES要件に追随し続けることは並大抵の苦労ではない。幸い,グローバルな非営利団体であるeClinical
Forumは,各国の規制・ガイドラインで要求されるシステム要件を40 件程度の要件に集約した“eCF
Requirements”を毎年更新しており,eClinical Forum のホームページ(https://eclinicalforum.org/download)から無償でダウンロードすることができる。
◆続きは「月刊PHARMSTAGE」2025年3月号 本誌でご覧ください◆
月刊PHARMSTAGEのホームページはこちら
https://www.gijutu.co.jp/doc/magazine_pharm%20stage.htm
参考文献
1)厚生労働省,「「「医薬品の臨床試験の実施の基準に関する省令」のガイダンスについて」の改正について」,
厚生労働省医薬・生活衛生局医薬品審査管理課長,薬生薬審発0705 第3 号,2019
|