|
1.はじめに
細胞外小胞 (EVs:Extracellular
vesicles) は,細胞から分泌される脂質二重膜構造を有する小胞の総称であり,タンパク質やマイクロRNA
(miRNA),メッセンジャーRNA (mRNA) 等の多種類の生体分子が内包された複雑な構造を有する。分泌細胞から標的細胞にこれらの機能性分子を送達したり,EV膜上のタンパク質が標的細胞の表面分子と相互作用したりすることで,EVは細胞間コミュニケーションの担い手となり種々の生体イベントに関与するとされており1),この機能を応用して新規の医薬品モダリティーとしての研究が現在活発に進められている。EVは産生経路やサイズによって数種類に分類され,後期エンドソームから多胞体を経て分泌される直径50-150
nm程度のエクソソーム,細胞膜から直接出芽する100-1000 nm程度のマイクロベシクル,アポトーシスの際に形成される数μmのアポトーシス小胞等が挙げられる。分泌後に各粒子の由来を特定することは困難であるため,国際細胞外小胞学会
(ISEV:International Society of Extracellular Vesicles)
が発出するポジションペーパー (MISEV2023:Minimal information
for studies of extracellular vesicles 2023) 2)では厳密な区別がつく場合を除いてEVもしくは細胞外微粒子
(EP:Extracellular particles) 等の包括的な呼称の使用が推奨されているが,EVの中でも最も生理機能の研究が進み,医薬品としての応用研究が先行しているエクソソームが本邦ではより一般的な呼称となっていることから,ここでは「エクソソーム」という呼称を使用させていただき,以下ではエクソソーム製剤の特徴について概説する。
エクソソーム製剤に使用されるエクソソームは,細胞から分泌されたエクソソームを精製・製剤化して使用する天然型と,遺伝子工学的手法もしくは物理的手法により薬理活性のあるタンパク質やRNA等を発現あるいは導入して使用する改変型の2種類に大別される。天然型としては特に間葉系幹細胞
(MSC) に由来するエクソソームが,MSC自体を細胞加工製品として投与した場合に治療効果を担う成分として注目されており,改変型ではエクソソームにmiRNAやタンパク質,ペプチド等を導入することで高血圧やがん等に対する治療効果をもたせた例が報告されている3)。目的物質を定義できる組換えタンパク質医薬品のような従来のバイオ医薬品に対してエクソソームは,タンパク質,核酸,リン脂質等,複数種類の生体分子によって構成される粒子が有効成分となる点が特徴である。また従来のバイオ医薬品では目的物質のアミノ酸配列は一義的に決定され,極めて高い純度の製剤が製造されているが,エクソソームは個々の粒子によってサイズや構成分子が異なる不均一な集団であり,また精製工程においてエクソソームをサイズや密度等が類似した別の種類のEVやリポタンパク質等から完全に単離することは難しく,これらの粒子は除去しきれず残存する可能性がある。培養上清由来の成分が薬理作用に関わる場合もあるとされ,その場合にはエクソソーム以外に活性成分が含まれる可能性を考慮した特性解析が必要となる。そのため,エクソソーム製剤の有効性と安全性を担保するためには,従来のバイオ医薬品での評価項目に加え,これらの粒子成分や,作用機序に応じて共存成分/不純物の評価・管理を行うことが必要となる。
2.エクソソーム製剤の品質管理戦略構築の概要
エクソソーム製剤の品質管理戦略の構築において,ICH
Q8:製剤開発,Q9:品質リスクマネジメント,Q11:原薬の開発と製造といった従来のバイオ医薬品の品質管理でも採用されているガイドラインを参照することができる。即ち,エクソソーム製剤として意図する有効性・安全性を達成するための製品品質の要約として目標製品品質プロファイル
(QTPP:Quality Target Product Profile) を設定し,QTPPを目標としたリスクアセスメントを実施する。QTPPを達成する上で一定の分布内・範囲内・限度内に管理が必要な特性を重要品質特性
(CQA:Critical Quality Attribute) として特定したうえで,製造工程の中でもCQAに重要な影響を及ぼす工程パラメータを重要工程パラメータ
(CPP:Critical Process Parameter) として特定する。原材料管理やCPPの適切な範囲での管理により,有効性・安全性確保を目標とした管理連略の構築が可能となる。エクソソーム製剤におけるQTPPとしては,製剤中のエクソソーム含量,保存安定性,剤形,投与経路等が想定され,CQAとしては粒子径分布,粒子数,電荷プロファイル,表面分子,生物活性,活性成分含量,不純物
(粒子様成分及び可溶性成分) 等が想定される。このようなアプローチは,製造実績に基づいて管理を行う従来の手法(traditional
approach)と対比して,より進んだ手法(enhanced approach)と呼ばれ,用いることは必須ではないが,製造スケールの変更等の製法変更を含め,製品ライフサイクルを通じて合理的な品質管理を行うには,有用な手法である。
管理戦略には,その構築に用いる手法によらず,(i)生産用の細胞基材や培地等の原材料の管理,(ii)培養,精製,加工等に関する各種工程パラメータの管理等の製造工程の管理と,(iii)製造された原薬や製剤の規格及び試験方法(出荷試験)が含まれる。エクソソームは前述の通り,現時点では精製による純度向上には限界があり,加えて非常に複雑な構造を有するため最終製品においてその特性全てを評価することは現実的には困難であることから,管理戦略における製造工程管理の重要性が高い。開発過程において,製品の品質特性と製造工程パラメータの関連に関する理解を深め,頑健性の高い製造工程を確立することが重要となる。
3.エクソソーム製剤の品質評価法(特性解析法)
他の医薬品の場合と同様に,エクソソーム製剤の管理戦略を構築する上では,開発過程において徹底的な特性解析を行うことが重要となる。本項では表1に示す特性解析項目の例の中でも,エクソソーム製剤に特有の項目を中心に,特性解析に用いる分析法について,各手法の特徴と留意点と紹介する。
表1 エクソソーム製剤の特性解析項目の例
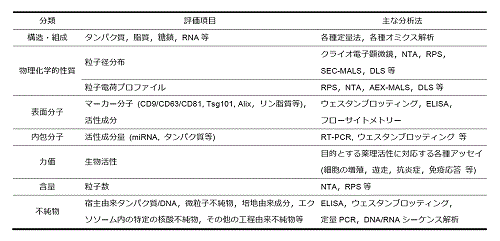
・粒子径分布
EVはその種類によって粒子径が異なり,EVの由来や投与後の体内動態や作用機序とも関連する可能性があるため,製剤中の粒子径分布の評価は重要な特性解析項目である。ナノサイズの粒子の粒子径分布の評価法として最も信頼性が高いとされる分析法は粒子画像を観察可能なクライオ電子顕微鏡や原子間力顕微鏡等による顕微鏡観察であり,エクソソーム製剤においても最も真値に近い値を得ることが出来る手法であるとされる2)。また,ナノ粒子の粒子径測定法として従来より動的光散乱
(DLS:Dynamic Light Scattering) が使用されてきたが,DLSは幅広な粒子径分布をもつサンプルを測定する際,散乱光の強度が高い大きい粒子の影響がより大きく,粒子径を過大に評価する傾向を有するため,サイズの異なる粒子の集団であるエクソソーム試料の測定には適していない。そこで現時点において,エクソソームを含むEV試料の粒子径分布を測定する手法として広く使用されているのがナノ粒子トラッキング解析
(NTA:Nanoparticle Tracking Analysis)である。NTAでは溶液中にレーザー光を照射した際に個々の粒子から発せられる散乱光を経時的に追跡することでブラウン運動を解析し,得られた拡散係数から流体力学径を算出する。同様に1粒子毎の粒子径を測定可能な手法としては抵抗パルスセンシング
(RPS:Resistive Pulse Sensing) が挙げられる。RPSではナノメートルスケールの細孔
(ポア) を挟んだ溶液中に電圧をかけ,溶液中のナノ粒子がポアを通過する際に発生する電気抵抗パルスの大きさから実粒子径を算出する。これらの測定法は1粒子毎に粒子径を計測可能なため,解像度の高い粒子径分布を得ることができる。
また,1粒子毎の粒子径測定とは異なるが,サイズ排除HPLC (SE-HPLC) もしくはフィールドフロー分画
(FFF:Field Flow Fractionation) と多角度光散乱 (MALS:Multi-angle
Light Scattering) 検出器を組み合わせたSEC-MALS及びFFF-MALSも粒子径分布の評価には有用である4,5)。MALSは静的光散乱を応用した測定法であり,フローセル中の溶液にレーザー光を当てた際に発せられる散乱光を多角度に配置した検出器で補足し,各角度における散乱光強度のパターンが粒子径によって異なるというMie散乱理論を利用して回転半径を算出する。MALS自体はDLSと同様にバルク状態の粒子径を測定する手法であるものの,SE-HPLCやFFFといったサイズ分画法及びUV等の他の検出法と組み合わせることで,各画分に存在する微粒子の粒子径分布や共存する他の成分に関する評価が可能となる。但し,MALSにおけるシグナル強度は粒子サイズに応じて大幅に増減するため,クロマトグラム上のピーク面積比が粒子数の比をそのまま表すのではないことに注意が必要である。
これらの手法はいずれも詳細な粒子径分布を可能とするものの,NTAやMALSでは散乱光の強度が低い一定サイズ以下の粒子の検出感度が著しく低下し,RPS法でも使用するポアの対象サイズ外の粒子は測定できないため,製剤中のすべての粒子を1種類の測定法で分析することは不可能である。加えて,各測定原理により算出される粒子径は流体力学径や回転半径など,それぞれ異なる種類となっている。そのため,測定法ごとに異なる平均粒子径や粒子径分布が得られることを念頭に置き,各測定法の特徴を把握したうえで目的に合った分析法を選択することが重要となる。
参考文献
1)Kalluri,R.&LeBleu,V.S.,Science,vol.367,eaau6977(2020)
2)Welsh,J.A.etal.,JExtracellVesicles,13,e12404(2024)
3)Van Delen, M. et al., J Extracell Vesicles 13,
e12458 (2024)
|