|
1.はじめに
製剤中のニトロソアミンの評価は,製薬業界の多くの研究者にとって大きな課題となっている。2018
年,欧州医薬品庁(EMA)は,ニトロソアミン不純物の混入による複数のバルサルタン製剤の回収を発表した。ニトロソアミンは遺伝毒性物質であり,発がん性がある,または発がん可能性がある物質に分類される1)。製剤からの摂取を通じた,6
種類のニトロソアミンの最大許容摂取量は26.5 〜 96 ng/ 日である2,3)。
ニトロソアミン不純物は,通常,原薬の製造に由来するか,または保存期間中の製剤内に形成される。原薬製造時に生成したニトロソアミンは,後続の工程,または追加の精製操作で除去することが可能である。しかし,最終製剤中に形成されるニトロソアミン類は除去することができない。第二級アミンなどの感受性の高い原薬の場合,適切な条件下(例えば,高温,酸性条件,液相)での亜硝酸塩などのニトロソ化剤と反応することにより,ニトロソアミンが形成される。図1
に第二級アミンが亜硝酸塩と反応してN −ニトロソアミンを生成することを示す。最終的には三酸化二窒素(N2O3)とニトロシルイオン(NO
+)がニトロソ化剤であるが,亜硝酸塩はこれらのニトロソ化剤の前駆体である。亜硝酸塩は一般的に低濃度で存在することを考慮すると,感受性の高い原薬のニトロソアミンの量は,製剤に蓄積した亜硝酸塩の量に比例すると予想される。
現在,製造販売業者(MAH)は,製剤中のニトロソアミン不純物の存在を低減するよう,規制当局から要請されている2-4)。米国食品医薬品局(FDA)とEMA
は,原薬および医薬品製造業者が従うべき3 段階のリスク管理戦略を提案している。第1 段階にはリスク評価の実施が含まれ,第2
段階は試験による特定されたリスクの確認であり,第3 段階は製剤中のニトロソアミン不純物の生成を防止および低減するために実施した変更を報告することである。
製薬メーカーによるリスク評価は,製造過程でのニトロソアミンの生成および汚染の潜在的な原因を評価できるように行われる必要がある。添加剤は,医薬品のリスク評価において潜在的リスク因子として考慮されるが,ニトロソアミン自体の存在リスクは極めて低い。しかし,多くの添加剤には微量の亜硝酸塩が含まれており,特定の条件下では最終的に製剤中でニトロソアミンが形成される可能性がある。そのため,添加剤のサプライヤーは,MAH
が最終製剤中のニトロソアミン不純物の存在リスクを評価できるよう,添加剤に関する十分な情報を提供する必要がある5)。
FDA とEMA のガイダンス文書には,ニトロソアミンの生成抑制を目的とした複数の軽減策が記載されている3,4)。これには,革新的な軽減戦略を検討することが推奨されるが,特に「製剤の処方設計」と「サプライヤーの適格性確認」の2
つが最も重要な戦略として挙げられている。
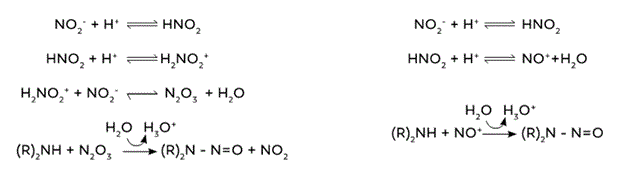
図1 第二級アミンからのN −ニトロソアミン生成経路
2.処方設計
添加剤を含む全ての製剤成分は,亜硝酸塩などのニトロソ化前駆体物質を含む可能性があり,これが製剤中のニトロソアミンの形成に寄与することがある。したがって,ニトロソアミンの形成を抑制するため,亜硝酸塩の量が低い添加剤を用いた処方改良が有効であると考えられる。また,アスコルビン酸又はα−トコフェロールなどの抗酸化物質を加えて,反応を抑制することも可能である6-8)。ただし,抗酸化剤は反応性が高く,原薬または製剤中の他の成分と相互作用する可能性があるため,阻害剤を用いた処方変更は慎重に検討する必要がある。また,ニトロソアミン生成は酸性条件下で促進されるため,製剤のpH
を上昇させることで生成速度を抑制できる8)。そのため,炭酸ナトリウムのようなpH
調整剤を配合することで,ニトロソアミンの形成を低減することも可能である。この場合,pH 調整剤が原薬の安定性に影響を与えないよう慎重に検討する必要がある。
3.サプライヤーの適格性確認
サプライヤーの適格性確認は,FDA ガイダンスにも記載されている重要な軽減戦略であり,医薬品の承認申請に対する影響を最小限に抑えながら実施できる。これは,亜硝酸塩の含有量が添加剤のロットやサプライヤーによって,著しく異なるという観察結果に基づくものである9)。多くの添加剤メーカーは,リスク評価のみに基づいて亜硝酸塩に関する情報を提供する。あるいは,データが入手可能な場合でも,感度の低い(すなわち,少量の亜硝酸塩が検出できない)分析方法で測定され,サプライヤー間の差異が明確に識別できない。さらに,様々なサプライヤーから入手した35
種類の添加剤のデータベースでは,亜硝酸塩と硝酸塩の濃度の相関は認められなかった9)。
モデル製剤においても,サプライヤーの選択がニトロソアミン生成に大きな影響を与えることが示された10)。Berardi
らは,亜硝酸塩の濃度が最も低い結晶セルロース,乳糖,スーパー崩壊剤などの添加剤を選択することで,潜在的なニトロソアミン生成を最大90%抑えることができることを報告した。さらに,カスタマイズされた製剤で形成されるニトロソアミンの理論量を計算するオープンアクセス計算ツールを提供した10)。本計算ツールは,サプライヤー選択がニトロソアミン生成リスクに及ぼす影響を定量的に評価するための手段として活用できる。
4 亜硝酸塩含有量に関する添加剤の種類とサプライヤーのベンチマーク
様々な添加剤で処方を変更するか,サプライヤーの適格性を評価するかにかかわらず,添加剤間,サプライヤー間,及びロット間の亜硝酸塩のばらつきの程度を評価するには,既存の科学文献は有用なツールとなる。初期の調査において,Wu
らは様々な賦形剤,スーパー崩壊剤,結合剤,滑沢剤,および流動化助剤において亜硝酸塩の含有量をスクリーニングした11)。その結果,亜硝酸塩の濃度は添加剤の種類およびサプライヤーに大きく依存するものの,亜硝酸塩は多くの添加剤に広く含まれていた。これは,処理水,酸滴定の手順,漂白および乾燥中の空気の酸化など,製造上の細かな違いによるものである。最近では,Lhasa
Limited 社が「添加剤の亜硝酸塩」データベースを構築し,その結果の一部がBoetzel
らの論文で紹介された。主な調査結果は,1)亜硝酸塩含有量の平均値とそのバラツキが添加剤によって大きく異なること,2)同じ種類の添加剤であっても,サプライヤーによって数値に大きな差があることであった9)。
賦形剤は,製剤に占める割合が大きいため,処方変更(すなわち代替添加剤への変更)またはサプライヤーの適格性評価(代替サプライヤーへの変更)が特に重要である。これらの添加剤に含まれる不純物の寄与は,崩壊剤,流動促進剤,および滑沢剤などの低用量成分より比較的高い。ただし,低用量の添加剤であっても,具体的な状況に応じて,適切に選択する必要がある。例えば,スーパー崩壊剤であるクロスポビドンは,賦形剤である結晶セルロースや乳糖に比べて,亜硝酸塩の平均値が9〜
12 倍高い。したがって低用量にもかかわらず,クロスポビドンが製剤全体に亜硝酸塩濃度上昇に大きく寄与する可能性が考えられる。そのため,感受性の高い原薬の処方においては,クロスポビドンをクロスカルメロースナトリウム(亜硝酸塩含有量の平均値がクロスポピドンの約15
分の1 である)で置き換えることが有効な選択肢となり得る9)。
さらに同じ種類の添加剤であっても,サプライヤーによって不純物にばらつきがある。表1 は,Boetzel
らの報告による結晶セルロースのサプライヤー8 社の亜硝酸塩含有量の中央値を示す。サプライヤーによって亜硝酸塩の含有量は大きな差異があり,最大で16
倍以上の変動が認められた。なお,サプライヤーごとに検体数が異なる点に留意する必要がある。詳細については,原論文をご参照頂きたい9)。
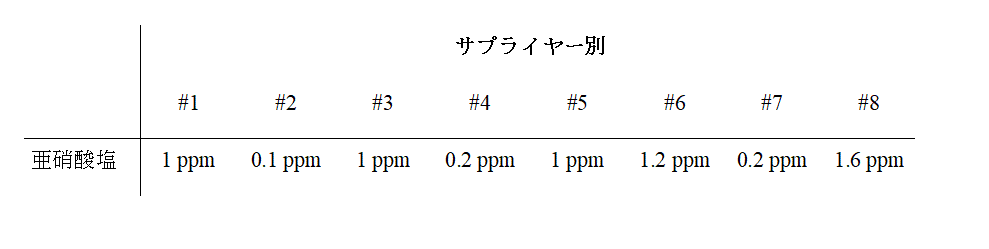
表1 各社の結晶セルロースにおける亜硝酸塩の含有量(ppm
=μg/g)9)
◆続きは「月刊PHARMSTAGE」2025年3月号 本誌でご覧ください◆
月刊PHARMSTAGEのホームページはこちら
https://www.gijutu.co.jp/doc/magazine_pharm%20stage.htm
参考文献
1)Brambilla, G., Martelli,
A. Genotoxic and carcinogenic risk to humans of
drug-nitrite interaction products. Mutation research,635,
17-52 (2007)
2)Questions and answers
for marketing authorisation holders/applicants
on the CHMP Opinion for the Article 5 (3) of Regulation
(EC) No 726/2004 referral on nitrosamine impurities
in human medicinal product, EMA/409815/2020 Rev.
11 (2022)
3)Control of Nitrosamine
Impurities in Human Drugs : Guidance forIndustry.
Cent. Drug Eval. Res., US FDA, Silver Spring,
MD, USA(2021)
4)Nitrosamine impurities,
EMA (2022)
5)The Role of Excipients
in Determining N-Nitrosamine Risks for Drug Products.
IPEC Federation (2022)
6)Mergens W. J. Efficacy
of vitamin E to prevent nitrosamine formation.
Annals of the New York Academy of Sciences, 393,61-69
(1982)
7)Nanda, K. K., Tignor,
S., Clancy, J., Marota, M. J., Allain, L. R.,
D’Addio, S. M. Inhibition of N-nitrosamine formation
in drug products : a model study. Journal of pharmaceutical
sciences, 110,3773-3775 (2021)
8)Ziebarth, D., & Scheunig,
G. Effects of some inhibitors on the nitrosation
of drugs in human gastric juice. IARC scientific
publications, 14, 279-290 (1976)
9)Boetzel, R., Schlingemann,
J., Hickert, S., Korn, C., Kocks, G., Luck, B.,
Blom, G., Harrison, M., Francois, M., Allain,
L., Wu, Y., Bousraf, Y. A Nitrite Excipient Database
: A useful Tool to Support N-Nitrosamine Risk
Assessments for Drug Products. Journal of pharmaceutical
sciences, 112, 1615-1624 (2023)
10)Berardi, A., Jaspers,
M., Dickhoff, B. H. J. Modeling the Impact of
Excipients Selection on Nitrosamine Formation
towards Risk Mitigation。 Pharmaceutics, 15, 2015
(2023)
11)Wu, Y., Levons, J.,
Narang, A. S., Raghavan, K., Rao, V. M. Reactive
impurities in excipients : profilinition (2010)
|