|
1.はじめに
今般,国内で輸入,製造,使用されている化学物質は数万種類にのぼる。
労働者が化学物質に曝露する機会は,製造・加工等の現場での蒸気や粉塵等の吸入による曝露と,皮膚への直接接触による曝露が多い。化学物質や医薬品を取り扱う職場において労働者の健康と安全を保護することは,各国の労働安全衛生政策の重要な優先事項であり,事業者の義務でもある。本稿では,そのための指針の1つとなる職業曝露限界(OEL)の設定と運用について概説する。
2.OELについて
各国において規制当局や公的機関等により,物質固有の十分な毒性情報に基づいてOELが設定,公開されている。数万種類の化学物質には有害性が不明な物質が多く含まれており,有害性がわかっている物質の中でもOELが設定されているのはごく一部に過ぎないが,有害性情報の蓄積や新しい物質の使用などに応じてOELは改訂・追加されている。
世界で最も影響力のあるOELは米国産業衛生専門家会議(ACGIH)の時間加重平均曝露限界(TLV-TWA)である。労働衛生学は1930年代に米国で始まり,1946年にACGIHによる最初のTLVリストが発行された。ACGIHのTLVは1950年代以降,多くの国で採用されている。日本においては,産業衛生に関する学術団体である日本産業衛生学会が1960年代から許容濃度等の勧告を行っている。現在,ACGIHでTLV-TWAが設定されている物質数は約8001),日本産業衛生学会で許容濃度が設定されている物質数は約2502)である。
また,厚生労働省はこれらのOEL(TLV, 許容濃度)とは異なるものとして,作業環境技術の実用可能性を考慮した「管理濃度」を設定している。さらに,2012年に印刷事業場の労働者に,当時は規制対象外であったジクロロプロパンによる胆管がんが発生したことを契機に,労働安全衛生法が改正され,その後の2022年の労働安全衛生規則等の改正を経て,3000物質超を目標に,厚生労働省が「濃度基準値」を設定しているところである。対象は,まず安衛法におけるリスク評価対象物質,次いで対象物質以外でOELがあり,かつ測定・分析方法があるもの,その後,OELはあるが測定・分析方法がないもの,という優先順位で計画されており,個々の物質の濃度基準値及び短期曝露限界値(STEL)の設定理由については,厚生労働省ホームページに各種資料が公開されている。
2.1 さまざまなOEL
OELは吸入経路に対する濃度の基準値として設定される。経皮曝露も特定の化学物質に関しては重要であるが,経皮曝露量は作業環境中の濃度と必ずしも相関するものではなく,経皮経路のみによる曝露量を直接測定する方法がないため,経皮OELは設定されない3)。OELとしては以下に示すいくつかの値が設定される。
(1)許容濃度 / TLV-TWA
OELは通常,標準的な労働時間(1日8時間,週40時間,40年間)における時間加重平均値(TWA)として設定される。平均曝露濃度がこの数値以下であれば,ほとんどすべての労働者に健康上の悪い影響が見られな
いと判断される濃度である。濃度測定値の時間加重平均値は以下の式により算出される。
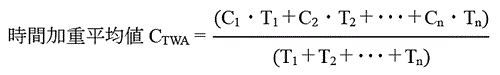
T1, T2, …, Tn
: 濃度測定における測定時間
C1, C2, …, Cn
: それぞれの測定時間に対する測定値
(2)短期曝露限界値(STEL)
8時間のTWAだけでは労働者を十分に保護できない化学物質がある。STELはこのような物質の曝露限界値として,通常は15分間に対して設定される。典型的な例は,呼吸器感作,刺激あるいは麻酔作用などの急性の有害影響を引き起こす化学物質である。STELが設定されている場合,TWAとSTELの両方を遵守する必要がある。ACGIHでは,STELが設定されていない場合の一時的な上昇について,1
回につき15分以内, 1日の就業時間内に60分以上の間隔を開けて4回以内,TLV-TWA の3倍の値を超えないこと,また,15分間のTWAとして測定した場合,いかなる状況でもTLV-TWAの5倍の値を超えないこと,とされている1)。
(3)天井値(Ceiling) /最大許容濃度
作業中のどの時間をとっても曝露濃度がこの数値以下であれば,ほとんどすべての労働者に健康上の悪い影響が見られないと判断される濃度であり,天井値が設定されている物質は作業中のいかなる時点でもそれを超過してはならない。天井値を超える曝露があるかどうかを判断するには,瞬間的な濃度の上昇を捉えることのできる測定技術が必要である。
(4)生物学的モニタリング
労働の場において,予防すべき影響の発生を予測・警告するために,有害物質に曝露している労働者の尿,血液等の生体試料中の当該物質あるいはその代謝物濃度等を測定することを,生物学的モニタリングという。ACGIHの勧告値であるBEI(生物学的曝露指標)は,体外的な曝露に対する勧告値であるTLV-TWAの濃度に対応する生体試料中の測定対象の濃度である1)。一方,日本産業衛生学会は,生物学的モニタリング値がその勧告値の範囲内であれば,ほとんどすべての労働者に健康上の悪い影響がみられないと判断される濃度として,生物学的許容値を勧告している2)。
(5)注釈
皮膚から吸収される化学物質の「皮膚(Skin)」注釈,経皮感作物質または呼吸感作物質の「皮膚感作(DSEN)」「呼吸器感作(RSEN)」注釈などが,OELに対して追加される。
化学物質が皮膚からも吸収され,全身の曝露が増加する可能性があるとき,OELが非常に低い場合は皮膚吸収が相対的に大きな影響を与える。例えば,皮膚が液体と接触している状況では,空気中の濃度をOEL未満に抑えても労働者を十分に保護しない可能性がある。
通常,皮膚への曝露がOELでの吸入曝露による体内負荷量の約10%以上を占めると想定される場合に,「皮膚(Skin)」注釈が適用される3)。OELは,経皮吸収がないことを前提として提案されている数値であることに注意する必要がある。なお,「皮膚(Skin)」注釈は経皮吸収の可能性に対するものであり,腐食性,刺激性,感作性など,皮膚への直接的な影響を警告するものではない。
2.2 OEL利用上の注意
OELが設定されている物質について,作業環境中の濃度をOEL以下に保つだけでなく,可能な限りばく露を最小限に抑えることが望ましい。
日本産業衛生学会は,許容濃度等の勧告2)の冒頭に以下の注意事項(抜粋)を掲げている。OELは想定された労働時間あるいは労働強度を超える場合には適用できず,労働の場以外での環境要因の許容限界値として用いることはできない。また,OELの数値を単純に毒性の強さの比較の尺度として用いてはならない。労働者に何らかの健康異常が見られた場合に,OELを超えたことのみを理由としてその物質による健康障害と判断するとか,逆にOELを超えていないことのみを理由としてその物質による健康障害ではないと判断してはならない。
また,各職場の労働衛生管理者だけでなく,OELを使用する全ての者は,取り扱う物質のOELの設定根拠を理解しておく必要がある。ACGIHはTLVリストの序文の中で,産業衛生学分野の訓練を受けた者のみが
TLVを使用すべきであると強調している1)。
3.医薬品のOEL
医薬品は,公的機関によりOELが設定されているものが少なく,臨床試験及び非臨床試験データに基づいて,事業者が設定する必要がある。近年は抗がん剤など高活性物質の比率が増えてきているため,医薬品製造現場における曝露リスクの確実なコントロールが増々重要になっている。
3.1 OELの算出手順
OELは,1日曝露許容量(PDE, ADE,
TDIなど)と同様に健康ベース曝露限界値(HBEL)4)の1つである。従って,基本的にはヒトの健康に有害な影響を及ぼさない用量・濃度に基づいて設定される。OELが環境汚染物質や医薬品の1日曝露許容量と異なるのは,曝露経路が吸入であること,値が空気中の濃度で表されること,対象集団として就業年齢の健康な成人が想定されることである。
ヒトあるいは動物の吸入毒性試験の情報が利用できる場合は,労働者の吸入推定無影響レベルを算出し,それをOELとして使うことができる5)。
利用できる吸入毒性データがない場合,非変異原性物質についてはその他の適切な毒性試験情報に基づき,以下の算出式によりOELを求めることができる。その際,算出の根拠となった試験の情報や,選択した係数F1〜F5の理由等を報告書に記録しておくことが望ましい。なお,ニューモダリティ医薬品においては,作用機序の点から必ずしも下式による機械的な算出が適切でない場合もある。OELの算出には,毒性学,薬理学,またはリスク評価の専門知識及び経験を有する者が関わる必要がある。
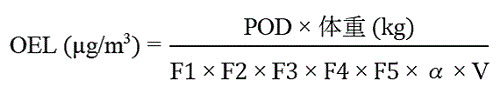
POD: Point of Departure (OEL算出の起点となる用量,単位 : mg/kg)
体重: 労働者の体重として60kg6)または70kg5)※1日曝露許容量(PDE)では,小児や高齢者,患者を含む一般集団の体重として50kg7)が用いられる。
F1: 種差の係数(1〜10)
ヒトの情報に基づく場合は1。
化学物質の曝露許容量算出では多くの機関がデフォルト値として10を使用しているが,医薬品を対象とするICH
Q3ガイドラインでは動物種ごとの体表面積に基づく係数(2〜12)を7),
EU REACH (欧州の化学物質の登録,評価,認可及び制限に関する規則)では代謝スケーリングに基づく係数(1.4〜7)に2.5を乗じた数値を使用している5)。
F2: 個体差の係数
デフォルト値は10とされることが多いが,対象集団が概ね健康な成人であることから,36)あるいは55)が選択されることもある。また,化学物質固有調整係数(CSAF)8)が使用できる場合もある。
F3: 試験期間の補正のための係数(1〜10)
F4: 影響の重篤性を考慮する係数(1〜10)
F5: 無影響量(NOEL)または無毒性量(NOAEL)が不明な場合に適用される係数(1〜10)
α: 投与経路間のバイオアベイラビリティ補正係数
V : 軽作業時の成人の8時間呼吸量 10m3
3.2 毒性データが無い場合
医薬品の開発段階によっては,OELを設定するための十分な毒性情報が得られていないものがある。そのような医薬品に対しては,ECETOC(欧州化学物質生体毒性・毒性センター)のデータが乏しい物質のためのOEL導出ガイダンス6)が参考になる。このガイダンスは化学物質のためのものであるが,暫定的なOELとして,リスクフレーズを用いたハザードバンディングによる方法,
LD50とlog KOWから最大耐量(MTD)を予測し,適切な評価係数を適用してOELを推定する方法,LC50
から算出する方法,類似の活性部位をもつ物質グループからのリードアクロスにより推定する方法,刺激性物質についてはRD50(呼吸数が50%減少する濃度)から推定する方法,毒性学的懸念の閾値(TTC)を利用する方法などが説明されている。
暫定的なOELを設定した医薬品については,開発段階が進んで毒性情報が得られた時点で,適切なOELを設定し直すことが望ましい。
参考文献
1)ACGIH, TLVs and BELs based on the documentation
of the Threshold Limit Values for chemical substances
and physical agents and biological exposure indices,
(2024)
2)日本産業衛生学,許容濃度等の勧告(2023年度),産業衛生学雑誌,65 (5), 268-300
(2023)
3)ECHA, Guidance on information requirements and
chemical safety assessment Appendix to Chapter
R. 8 : Guidance for preparing a scientific report
for health-based exposure limits at the workplace,
Version 1.0, (2019)
4)PDE設定検討会編, “ゼロから学ぶHBEL!”, じほう, (2021),1-3
5)ECHA, Guidance on information requirements and
chemical safety assessment, Chapter R. 8 : Characterisation
of dose [concentration]-response for human health,
Version : 2.1., (2012)
6)ECETOC, Guidance for Setting Occupational Exposure
Limits : Emphasis on Data-Poor Substances, Technical
Report No. 101, (2006)
7)ICH, ICH Harmonised guideline, Impurities :
Guideline for residual solvents, Q3C (R9), (2024)
8)WHO, Chemical-specific adjustment factors for
interspecies differences and human variability
: Guidance document for use of data in dose/concentration-response
assessment, Harmonization Project Document No.
2, (2005)
|